Wiskunde verklaart waarom Crispr-Cas9 soms het verkeerde DNA knipt
Wiskunde verklaart waarom Crispr-Cas9 soms het verkeerde DNA knipt
De ontdekking van Crispr-Cas9 is voor de medische wetenschap van grote waarde geweest. Het heeft gene editing vele malen eenvoudiger gemaakt, en gaat er mogelijk zelfs voor zorgen dat we in de nabije toekomst erfelijke ziekten uit onze genen kunnen wissen. Met Crispr-Cas9 zijn we in staat om DNA in een cel open te knippen om gemuteerde genen te repareren, of om nieuwe stukken DNA op de geopende plek te plakken. In eerste instantie leek het systeem extreem nauwkeurig te zijn. Maar inmiddels is duidelijk dat Cas9 soms ook knipt in DNA-sequenties die lijken op de sequentie waar het eiwit naar op zoek is. Wetenschappers van de TU Delft hebben een model ontwikkeld dat verklaart waarom Cas9 de ene DNA-sequentie kapot knipt en de andere met rust laat.
Het Crispr-Cas9-systeem is een verdedigingsmechanisme dat bacteriën beschermt tegen virussen. Als een virus een bacteriecel binnendringt maar de cel niet weet over te nemen, knipt het verdedigingssysteem met een moleculair schaartje wat genetisch materiaal uit het virus. Vervolgens bouwt het dat erfelijk materiaal in het DNA van de bacterie in. Het ingebouwde virale DNA fungeert als een soort genetisch geheugen. Als hetzelfde virus de bacterie (of diens nazaten) later nog eens aanvalt, herkent de bacterie de aanvaller en kan hij er het Cas9-eiwit op af sturen. Met virus-RNA als ‘spiekbriefje’ gaat het eiwit op jacht naar vijandig DNA in de cel. Vindt het een match, dan knipt het Crispr-Cas9-systeem het virale DNA kapot.
Schadelijke gevolgen
Wetenschappers dachten in eerste instantie dat Crispr-Cas9 alleen knipt als een stuk DNA exact overeenkomt met het ‘spiekbriefje’ van RNA dat het bij zich heeft. Helaas blijkt dat niet zo te zijn. Het eiwit knipt soms DNA-sequenties die wel lijken op het materiaal waar het naar op zoek is, maar die een aantal afwijkende letters bevatten. Volgens onderzoeker Martin Depken van de TU Delft is dat knippen van andere sequenties vanuit evolutionair oogpunt heel logisch. ‘Virussen muteren continu, en kunnen dus net ander DNA hebben dat waar Crispr-Cas9 naar op zoek is. Door ook DNA-sequenties te knippen die net iets afwijken, kan het eiwit de evolutie van een virus volgen en de cel beter tegen virussen beschermen.’
Maar wat goed is voor bacteriën, is in dit geval heel slecht voor mensen. Als we Cas9 namelijk willen gebruiken als instrument om ziekten mee uit ons DNA te schrijven, kan het schadelijke gevolgen hebben als het eiwit onze genen ook op andere plekken kapot knipt dan op de bedoelde plek.
Beloond met energie
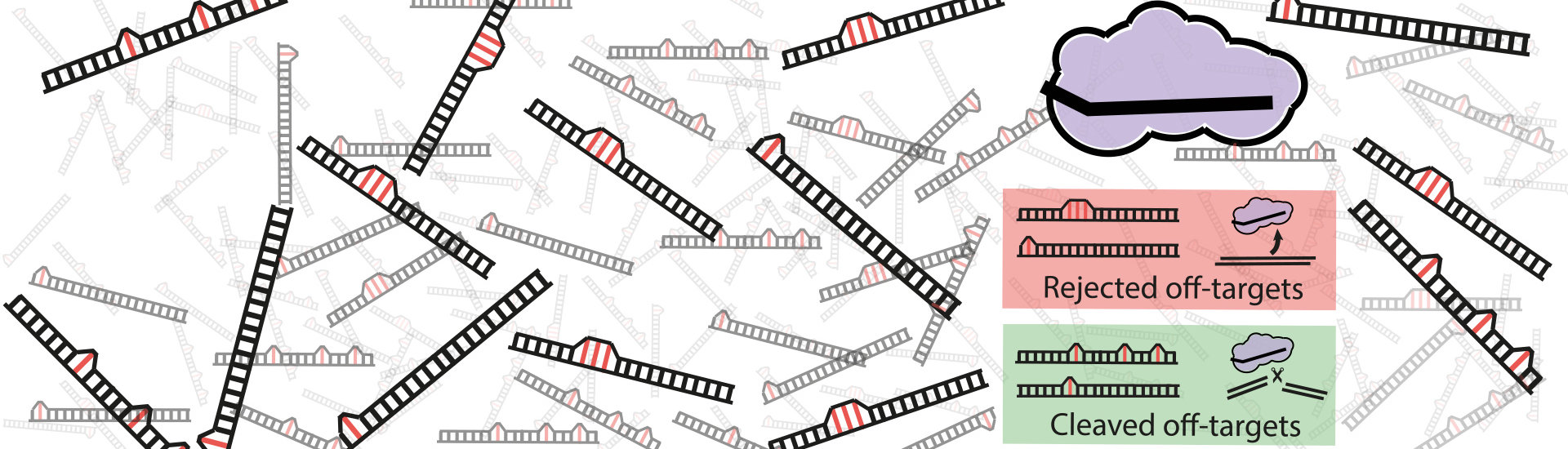
Uit experimenten is gebleken dat Crispr-Cas9 geneigd is om eerder in bepaalde niet-kloppende sequenties te knippen dan in andere. Wetenschappers van de onderzoeksgroep van Martin Depken, onder leiding van PhD-student Misha Klein, vroegen zich af wat de onderliggende fysica is die deze voorkeur bepaalt. Het antwoord is volgens Depken heel simpel: het draait om de energie die het kost om basenparen te maken die afwijken van het RNA-spiekbriefje. ‘Als Cas9 checkt of een DNA-sequentie een match is, begint het aan één kant van de streng’, legt hij uit. ‘Vervolgens loopt het alle letters van de streng af om te kijken of er een match is.’ Voor elk juiste paar wordt het eiwit beloond met energie. Alle zogeheten mismatches kosten energie. Hoe meer ‘fouten’ er in de sequentie zitten, en hoe dichter ze bij het begin van de streng zitten, des te groter de kans is dat het eiwit niet tot knippen overgaat. Het laat dan weer los en gaat op zoek naar een stuk DNA dat beter overeenkomt met zijn RNA-template.
Betere voorspellingen
Het eenvoudige wiskundige model dat de wetenschappers hebben ontwikkeld, voorspelt het knipgedrag van Cas9 volgens Depken verbazingwekkend goed. Als een fout aan het einde van een DNA-sequentie zit, heeft het eiwit genoeg energie verzameld om de horde te nemen, en is de kans dus groter dat het gaat knippen. Het model verklaart ook waarom Cas9 niet knipt wanneer het eiwit een mismatch aan het begin van een streng tegenkomt, of wanneer twee foutjes dicht op elkaar zitten.
De natuurkundige eigenschappen van het Cas9-eiwit hebben zelf eveneens invloed op de ‘knipkans’. Depken en zijn collega's willen deze variabele nu ook in hun model opnemen. Uiteindelijk moet het model leiden tot betere voorspellingen van de fouten die Cas9 waarschijnlijk maakt in verschillende scenario’s. ‘Soms kunnen we bij het repareren van een gen meerdere plekken kiezen om te knippen. Ons model zal helpen bepalen welke locaties het beste doelwit zijn', zegt Depken. Het fysische inzicht dat het model verschaft kan eveneens bijdragen aan pogingen om het Cas9-eiwit zo te verbouwen dat het eiwit geen levensbedreigende fouten maakt terwijl het ons DNA herschrijft.
*****
Meer informatie:
‘Hybridization kinetics explains CRISPR-Cas off-targeting rules’, Misha Klein, Behrouz Eslami-Mossallam, Dylan Gonzalez Arroyo, Martin Depken, Cell Reports
DOI: 10.1016/j.celrep.2018.01.045
Martin Depken (Assistant Professor)
+31 (0)15 27 81305
S.M.Depken@tudelft.nl
Zie ook: onderzoeksverhaal ‘Sleutelen aan het Leven’ over Crispr-Cas9 (TU Delft)